Соблюдение требований ЕАЭС для регистрации лекарственных препаратов до конца 2025 года
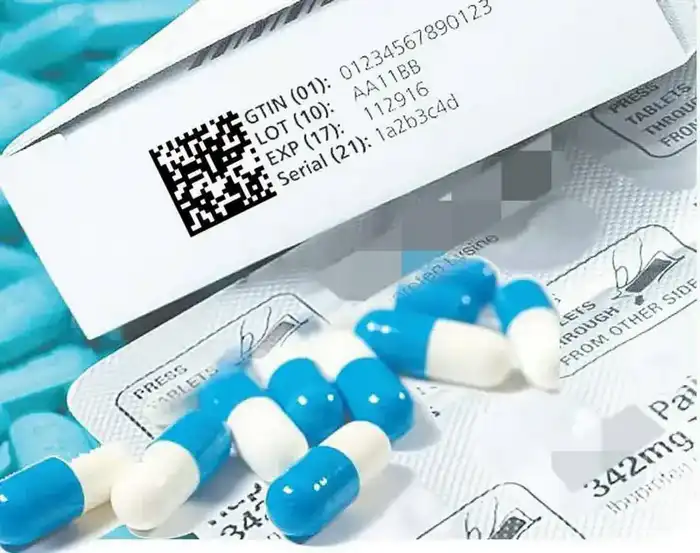
Внимание всем производителям и держателям регистрационных удостоверений! С 31 декабря 2025 года все лекарства, зарегистрированные в нашей стране, должны соответствовать новым требованиям ЕАЭС. Если не успеете привести препараты в соответствие, это может привести к отказу в регистрации.
Заявления на приведение в соответствие будут приниматься до конца 2025 года. При этом не потребуется предоставление полного досье в формате CTD. Важно указать Казахстан в качестве референтного государства или государства признания при подаче заявления.
Сроки и требования
Полное регистрационное досье необходимо предоставить до 31 декабря 2026 года. Экспертные работы начнутся только после получения полного досье. Если досье не будет предоставлено, регистрация не состоится.
Срок действия регистрационного удостоверения может быть продлён на время процедуры, если будет подано соответствующее заявление и документы. Однако данное уведомление не касается препаратов, зарегистрированных по Решению Евразийской экономической комиссии от 10 июня 2022 года №96, а также стратегически важных лекарств, которые приводятся в соответствие добровольно.
В случае, если какие-либо препараты не будут приведены в соответствие с требованиями ЕАЭС, необходимо направить их перечень в КМФК, а также предоставить копию в НЦЭЛС.